新型抗埃博拉病毒病靶点研究进展
埃博拉病毒病是由纤丝病毒科(filoviridae)的埃博拉病毒(Ebola virus,EBOV)所引起的一种急性出血性传染病,该病病死率极高,达50%-90%, 是人类最致命的病毒性传染病之一。世界卫生组织统计数据显示,在2013年底至2015年西非埃博拉疫情大爆发中超过22500人感染埃博拉病毒,因感染丧生的人数达9000人。不论是感染病例数量、死亡人数,还是受影响地区范围,都达到了该病毒1976年被发现以来的最大规模。2014年8 月8 日,EBOV 的爆发被正式做为国际高度关注的突发公共卫生事件。目前,世界各国都没有有效控制埃博拉疫情的药物和治疗方法。
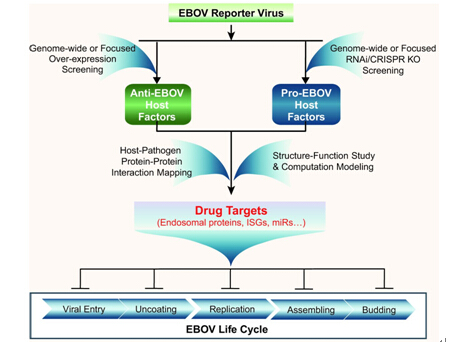
NSR新近发表了由中国医学科学院苏州系统医学研究所秦晓峰教授、蒋太交教授、程根宏教授和中国医学科学院协和医学院基础医学研究所蒋澄宇教授的联合撰文“New targets for controlling Ebola virus disease”(http://nsr.oxfordjournals.org/content/2/3/266.full)。该文结合埃博拉病毒生命周期,从病毒入侵、宿主释放可溶性蛋白等角度分析了25-羟基胆固醇(25-hydroxyl cholesterol,25HC)等天然免疫抗病毒小分子化合物对埃博拉病毒的潜在抑制作用,从预防埃博拉病毒感染角度阐述了新的药物靶点的研究战略进展,运用系统生物学方法阐述了病原体-宿主之间的相互作用。
文章首先介绍了靶向埃博拉病毒入侵宿主细胞过程的小分子抑制剂的研究进展。不同于其他包膜病毒,埃博拉病毒是通过诱导细胞启动微胞饮(Macropinocytosis)作用而侵入细胞内部。最近研究显示,two-pore channel(TPC)蛋白家族在埃博拉病毒入侵宿主细胞的过程中扮演着重要角色,而小分子化合物Tetrandrine能够潜在特异性地抑制TPC通道,从而阻碍病毒的入侵过程。因此,类似于TPCs,靶向病毒入侵的其他小分子抑制药物还有待进一步研究发现。同时,宿主编码的干扰素诱导ISG蛋白具有强烈的抗病毒感染天然免疫效应功能。作者实验室研究结果显示胆固醇-25 羟化酶(Cholesterol-25-hydroxylase,CH25H)能够将胆固醇转化成一种可溶性因子-25 羟基胆固醇(25HC)。在P-4生物安全等级研究中证明25HC可显著降低野生型EBOV(Zaire Strain,扎伊尔株)对人体细胞的感染,显示其具有作为新型抗埃博拉病毒感染的紧急治疗药物的巨大潜力。
除了靶向病毒入侵过程,文章还描述了靶向病毒出芽从宿主细胞脱落、感染细胞释放可溶性蛋白过程的药物研究进展。其中,埃博拉病毒GP蛋白,无论是覆盖在病毒表面,还是在感染过程中从受感染细胞脱落,都可以参与多种免疫应答反应,在病毒生命周期以及宿主-病原体相互作用过程中扮演重要角色,是抑制埃博拉病毒侵染、复制、发病过程的潜在有效靶点。
目前,为国家抗击EBOV 病毒侵染、传播的小分子药物应急战略储备,研制和制备高效、安全且能快速效治疗埃博拉病毒的药物迫在眉睫。针对不同靶点的小分子抑制药物,进一步阐明埃博拉病毒病的发病机理还有待进一步研究。

 打印本文
打印本文 关闭窗口
关闭窗口