老年痴呆模型/阿尔茨海默症模型/AD模型
老年痴呆动物模型
1、APP/PS1双转基因小鼠
转入人源β-淀粉样蛋白前体(APP)基因的小鼠表现出Aβ相关病理特征,引入PS1基因的APP/PS1双转基因小鼠相较于APP转基因小鼠,Aβ沉积和老年斑形成速度加快,学习记忆障碍显著提前,伴有神经元丢失、胶质增生和突触丢失等改变,是研究阿尔兹海默症的理想模型,导致早发型老年痴呆症。4月龄出现老年斑SP,6月龄出现Aβ沉积,10-12月龄出现记忆相关的行为学障碍。
应用:由于APP/PS1双转基因小鼠无法形成NFTs,适合用于靶向Aβ药物的非临床评价。
缺点:无神经退行性病变、脑萎缩和TNFs。
2、SAMP8小鼠 – 自发型衰老模型
SAM小鼠(Senescence accelerated mouse)呈现出加速衰老的表型,包含一系列近交品系,可分为P系和R系,P系为快速老化小鼠(Senescence accelerated mouse/prone, SAMP),4-6月龄时出现反应迟缓、学习记忆功能障碍等老化特征;R系为抗快速老化小鼠,作为SAMP的正常对照。SAMP8亚系与正常小鼠相比,寿命更短、学习和记忆能力不足,在增龄过程中,APP表达水平显著升高,大脑中呈现出类似人类Aβ和Tau病理学特征,伴有氧化损伤、乙酰胆碱转移酶活力降低等人类AD相关病理特征。
应用:广泛用于阿尔茨海默症和其他衰老相关疾病的机制和新药开发研究。自发表现出AD相关的病理改变,接近临床病程改变,尤其适合抗散发性阿尔茨海默症新药的非临床研究。
缺点:均一性较差、费用昂贵;很少出现Tau相关病理改变,不适合以Tau为药物靶点的新药研发。
3、东莨菪碱诱导模型 – 中枢胆碱系统损伤模型
东莨菪碱属于胆碱能拮抗药物,能穿过血脑屏障,抑制乙酰胆碱与受体结合,引发中枢胆碱系统紊乱,造成动物短期学习记忆障碍,可模拟AD患者行为的异常表现。向小鼠腹腔单次或多次注射东莨菪碱可引起脑内乙酰胆碱(ACh)水平显著下降,诱导AD动物模型。单次给药30min后即可出现明显学习记忆障碍,连续注射4周后,大鼠脑内Aβ和异常磷酸化Tau蛋白含量明显升高。
应用:适用于研究AD模型中的认知障碍和相关药物评价。
缺点:1、痴呆症状可逆;2、东莨菪碱对中枢M受体阻断为非特异性,动物可能出现焦虑、行动迟缓、自主活动增多等干扰行为学评价的不良反应。
动物种属
小鼠、大鼠
评价指标
1、神经行为学检测: Morris水迷宫实验(定位航行实验、空间探索实验)、避暗实验、新物体识别、巴恩斯迷宫、社交箱、旷场、转棒仪、高架十字迷宫等;
2、Aβ检测:1)ELISA检测Aβ含量(组织匀浆、血浆、脑脊液);2)老年斑组织染色(免疫组化);
3、Tau蛋白检测:WB法测定脑内过磷酸化Tau蛋白水平;
4、病理免疫组化:1)神经元数量;2)小胶质细胞数量;3)星形胶质细胞数量;4)NFTs;
5、大脑海马和皮层中AChE、ChAT活性及ACh含量测定,ELISA(东莨菪碱诱导模型);
6、神经炎症检测;
7、氧化应激检测。
案例展示
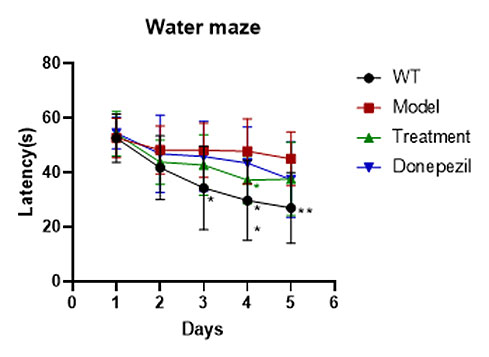
阿尔茨海默症模型:APP/PS1双转基因小鼠
欢迎联系我们,共同探讨您的抗老年痴呆症新药研发项目,体验我们的服务。
相关技术资料
运费说明


























